1 Epidemia dengi Tło: Rosnące globalne wyzwanie dla zdrowia publicznego
Denga to ostra choroba wirusowa przenoszona przez komary, wywoływana przez wirus dengi (DENV), który stał się najszybciej rozprzestrzeniającą się chorobą arbowirusową na świecie, stanowiącą poważne zagrożenie dla bezpieczeństwa zdrowia publicznego. W ciągu ostatnich dwóch dekad globalna zapadalność na dengę dramatycznie wzrosła, a liczba zgłaszanych przypadków podwaja się corocznie od 2021 r. [1]. W grudniu 2023 r. Światowa Organizacja Zdrowia (WHO) ogłosiła globalny stan wyjątkowy w związku z dengą w celu wzmocnienia skoordynowanych międzynarodowych działań reagowania. Szacunki epidemiologiczne WHO wskazują, że około 3,9 miliarda osób na całym świecie jest narażonych na zakażenie dengą, przy czym szacuje się, że rocznie występuje 390 milionów zakażeń — z czego 96 milionów to przypadki klinicznie jawne [1,2].
2 najważniejsze wydarzenia epidemiologiczne
Charakterystyka epidemiologiczna dengi jest kształtowana przez interakcję czynników wirusologicznych, ekologii wektorów, odpowiedzi immunologicznej gospodarza oraz warunków społeczno-środowiskowych. Kompleksowe zrozumienie tych cech jest niezbędne do opracowania skutecznych strategii zapobiegania i kontroli, a także trafnych metod diagnostycznych.
2.1 Wektory transmisji i wzorce transmisji miejskiej
Wirus dengi przenoszony jest głównie przezAedes aegypti i Aedes albopictusKomary. Spośród tych gatunków wektorów, Aedes aegypti jest uznawany za najbardziej krytyczny wektor transmisyjny, charakteryzujący się wysoką „zdolnością adaptacji człowieka” i szerokim występowaniem w tropikalnych i subtropikalnych środowiskach miejskich. W przeciwieństwie do innych komarów będących wektorami patogenów arbowirusowych, Aedes aegypti wykazuje następujące kluczowe cechy epidemiologiczne:
-Preferencja do rozmnażania się w środowiskach antropogenicznych (np. w zbiornikach na wodę, zużytych oponach)
-Silny tropizm dla krwi ludzkiej jako źródła składników odżywczych
-Zachowanie żywieniowe w ciągu dnia
Cechy te definiują dengę jako typową„miejska choroba zakaźna”ze znacznie zwiększoną skutecznością transmisji w obszarach gęsto zaludnionych. Badania prowadzone przez WHO wykazały, że w obszarach miejskich o dużej gęstości zaludnienia zwiększona częstotliwość kontaktu komarów z ludźmi może znacząco zwiększyć podstawowy współczynnik reprodukcji (R₀) wirusa DENV, przyspieszając w ten sposób rozprzestrzenianie się epidemii [2].
2.2 Globalne trendy rozprzestrzeniania się i czynniki napędzające
Według raportów WHO liczba zgłaszanych przypadków dengi na świecie wzrosła wykładniczo w ciągu ostatnich dwóch dekad [1,3]. Tendencja wzrostowa jest napędzana przede wszystkim przez następujące powiązane ze sobą czynniki:
(1) Zmiany klimatyczne: Rosnące temperatury globalne nie tylko poszerzają zasięg geograficzny odpowiednich siedlisk dla komarów-nosicieli, ale także skracają okres inkubacji wirusa DENV w żywicielu komara, zwiększając tym samym skuteczność transmisji. WHO potwierdziła, że zmiany w zagęszczeniu komarów wywołane zmianami klimatu stanowią wiarygodny predyktor dynamiki czasoprzestrzennej epidemii dengi.
(2) Urbanizacja: Szybka i nieplanowana ekspansja miejska stworzyła liczne siedliska lęgowe dla komarów przenoszących choroby, podczas gdy wzrost gęstości populacji wzmocnił ciągłość łańcuchów transmisji wirusa DENV.
(3) Globalny ruch ludności: Podróże i handel międzynarodowy ułatwiły szybką transmisję wirusa DENV przez granice, promując przejście od przypadków importowanych do trwałej transmisji lokalnej. Dane z monitoringu WHO pokazują, że w latach 2010–2021 w Stanach Zjednoczonych zgłoszono 7528 przypadków dengi związanych z podróżami, z czego 3135 wymagało hospitalizacji, a 19 zakończyło się zgonem.
(4) Ekspansja zasięgu wektorów: Na całym świecie zasięg geograficzny komarów Aedes aegypti i Aedes albopictus stale się rozszerza, a komary Aedes coraz częściej pojawiają się w niektórych częściach Europy. W rezultacie denga przekształciła się z tradycyjnej epidemii regionalnej w globalne zagrożenie dla zdrowia publicznego.
2.3 Mechanizmy współkrążenia i reinfekcji wielu serotypów
Wirus dengi obejmuje cztery antygenowo odrębne serotypy (DENV-1 do DENV-4). Zakażenie jednym serotypem zapewnia długotrwałą odporność ochronną przed tym konkretnym serotypem, ale jedynie tymczasową i częściową ochronę krzyżową przed pozostałymi trzema serotypami. Populacja ogólna jest uniwersalnie podatna na DENV, a jedynie u niewielkiej grupy zakażonych osób rozwija się choroba kliniczna [2].
W regionach endemicznych wiele serotypów wirusa DENV często krąży jednocześnie, co zwiększa ryzyko wystąpienia u osób wielu zakażeń wirusem denga w ciągu całego życia. Badania epidemiologiczne WHO wykazały, że współkrążenie wielu serotypów jest kluczowym czynnikiem powodującym okresowe epidemie denga [1].
2.4 Zakażenie wtórne i wzmocnienie zależne od przeciwciał
Krytycznym i wyjątkowym zjawiskiem w epidemiologii dengi jestwzmocnienie zależne od przeciwciał (ADE)Podczas wtórnego zakażenia heterologicznym serotypem wirusa DENV, przeciwciała nieneutralizujące wytwarzane podczas zakażenia pierwotnego ułatwiają wnikanie wirusa do monocytów i makrofagów, zwiększając w ten sposób jego replikację. Mechanizm ten jest powszechnie uznawany przez WHO za główny czynnik patogenny ciężkiej postaci dengi, w tym gorączki krwotocznej dengi i zespołu wstrząsu dengi [1].
Dane epidemiologiczne WHO konsekwentnie wskazują, że osoby z wtórnym zakażeniem wirusem denga mają znacznie wyższe ryzyko rozwoju ciężkiej postaci choroby w porównaniu z osobami z zakażeniem pierwotnym – cecha ta ma ogromne znaczenie dla monitorowania choroby i leczenia klinicznego. Należy zauważyć, że chociaż ryzyko ciężkiego przebiegu choroby jest podwyższone podczas zakażenia wtórnego, zakażenie dowolnym serotypem wirusa denga może potencjalnie rozwinąć się w ciężką postać choroby denga [1].
2.5 Niespecyficzne objawy kliniczne i ryzyko błędnej diagnozy
Objawy kliniczne dengi są wyjątkowo niespecyficzne, zwłaszcza we wczesnych stadiach choroby, często pokrywając się z objawami innych infekcji wirusowych przenoszonych przez komary (np. wirusów chikungunya i Zika), a także niektórych infekcji dróg oddechowych. Szacunki WHO wskazują, że 40–80% zakażeń wirusem DENV przebiega bezobjawowo [3].
Typowe objawy kliniczne obejmują:
-Ostra gorączka (utrzymująca się przez 2-7 dni, która może być dwufazowa)
-Silny ból głowy i ból zaoczodołowy (ból za oczami)
-Ból mięśni i stawów (często nazywany „gorączką łamiącą kości”)
-Wysypka plamista lub grudkowo-plamkowa
- Łagodne objawy krwotoczne (np. wylewy krwawe, krwawienie z nosa, krwawienie z dziąseł)
Objawowa denga zazwyczaj dzieli się na trzy odrębne fazy: fazę gorączkową, fazę krytyczną i fazę zdrowienia. Około mniej niż 5% pacjentów objawowych przechodzi w ciężką postać dengi. Ze względu na brak specyficznych objawów klinicznych, diagnoza oparta wyłącznie na objawach klinicznych jest trudna, co zwiększa ryzyko błędnej diagnozy i niedodiagnozowania. WHO wyraźnie podkreśla, że samo rozpoznanie kliniczne nie wystarcza do zapewnienia dokładności, dlatego niezbędne jest potwierdzenie laboratoryjne [1].
3 kluczowe punkty raportu WHO „Badania laboratoryjne na obecność wirusa dengi: tymczasowe wytyczne, kwiecień 2025 r.”
W kwietniu 2025 roku Światowa Organizacja Zdrowia opublikowała zaktualizowane tymczasowe wytyczne dotyczące badań laboratoryjnych w kierunku wirusa dengi (DENV), zawierające wiarygodne wskazówki techniczne dotyczące globalnej diagnostyki dengi. Wytyczne te syntetyzują najnowsze dane dotyczące badań laboratoryjnych w kierunku dengi w kontekście trwającego globalnego zagrożenia związanego z tą chorobą i przedstawiają praktyczne zalecenia dostosowane do środowisk o zróżnicowanym poziomie zasobów.

3.1 Podstawowe zasady strategii testowania
W wytycznych podkreślono, że diagnostyka dengi musi opierać się na wielomarkerowej strategii testowania, uwzględniającej stadium choroby [1]. Ze względu na brak uniwersalnego algorytmu diagnostycznego, strategie testowania powinny być dostosowane do lokalnych kontekstów epidemiologicznych, z uwzględnieniem następujących kluczowych czynników [1]:
- Etap zakażenia: Liczba dni po wystąpieniu objawów decyduje o wyborze najodpowiedniejszej metody badania
-Rodzaj próbki: przydatność pełnej krwi, osocza lub surowicy do wykrywania wirusa DENV
-Epidemiologia regionalna: Lokalnie krążące serotypy wirusa DENV i współkrążenie innych arbowirusów
-Ryzyko koinfekcji: W regionach, w których występuje nakładanie się arbowirusów, należy rozważyć wykonanie testów multipleksowych w celu rozróżnienia różnych patogenów
3.2 Strategia testowania oparta na etapach
Zgodnie z wytycznymi WHO badania laboratoryjne na obecność dengi powinny odbywać się w określonych przedziałach czasowych, zależnie od stadium choroby [1,2]:
(1) Badanie fazy ostrej (≤7 dni po wystąpieniu)
-Badanie kwasu nukleinowego (badanie molekularne): reakcja łańcuchowa polimerazy z odwrotną transkrypcją (RT-PCR) i inne metody molekularne pozwalają na wykrycie RNA wirusa DENV z wysoką czułością.
-Badanie antygenowe: wykrywanie antygenu NS1, który staje się wykrywalny w ciągu 1–3 dni od wystąpienia objawów.
W ostrej fazie poziom wiremii jest stosunkowo wysoki, a testy kwasu nukleinowego i antygenu osiągają optymalną czułość.
(2) Badanie fazy rekonwalescencji (≥4 dni po wystąpieniu objawów)
-Badania serologiczne: Przeciwciała IgM stają się zazwyczaj wykrywalne około 4 dnia od wystąpienia objawów.
- W większości przypadków przeciwciała IgM utrzymują się przez 14–20 dni, a w niektórych przypadkach okres ich występowania może wydłużyć się do 90 dni.
-Badanie IgG ma ograniczoną wartość w diagnostyce ostrej dengi ze względu na możliwość występowania przeciwciał krzyżowo reagujących z wcześniejszym zakażeniem flawiwirusem lub szczepieniem.
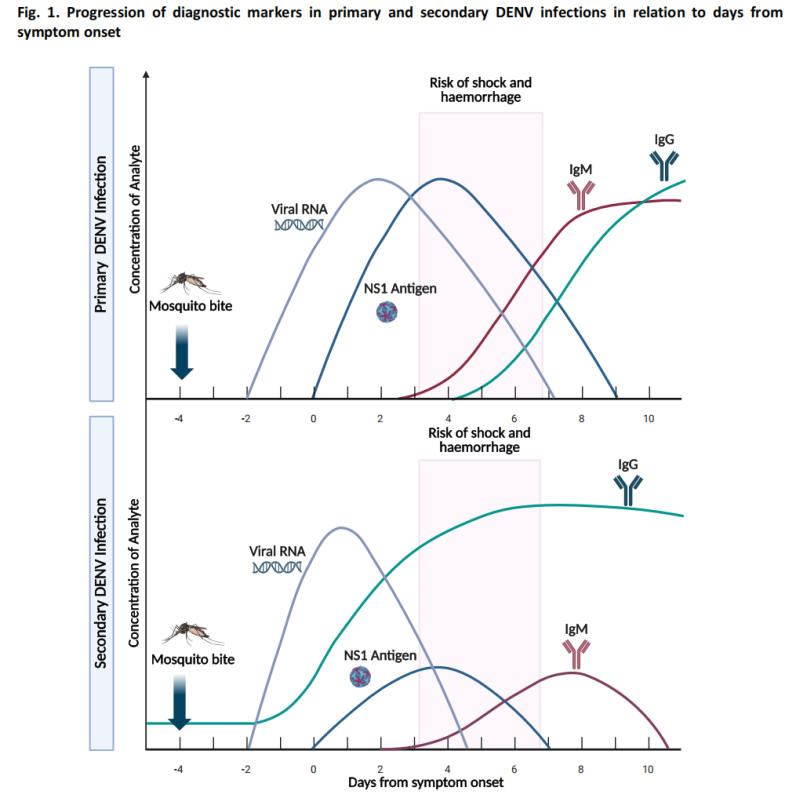
(3) Algorytm diagnostyczny podejrzanego przypadku
Wytyczne obejmują algorytm diagnostyczny dla podejrzewanych przypadków dengi, zalecający odpowiednie metody testowania w zależności od liczby dni po wystąpieniu objawów: badanie antygenu NS1 i badanie kwasu nukleinowego to główne podejścia we wczesnej fazie, podczas gdy badanie serologiczne to główna metoda w fazie późniejszej.
3.3 Ocena i wybór wydajności metody testowania
Według WHO systematyczna ocena skuteczności i możliwych scenariuszy różnych testów na obecność wirusa dengi przedstawia się następująco:
| Metoda testowania | Cel | Okno czasowe | Główny scenariusz zastosowania | Rozważania |
| Testowanie kwasów nukleinowych | Wirusowe RNA | 1-7 dni po wystąpieniu objawów | Wczesne potwierdzenie, identyfikacja serotypu | Metoda będąca złotym standardem; wymaga specjalistycznego sprzętu laboratoryjnego i wiedzy technicznej |
| Badanie antygenu NS1 | Białko niestrukturalne | 1-3 dni po wystąpieniu objawów | Wczesne szybkie badania przesiewowe | Dostępne w formacie szybkiego testu diagnostycznego (RDT), odpowiedniego dla środowisk o ograniczonych zasobach |
| Badanie przeciwciał IgM | Specyficzne przeciwciała IgM | ≥4 dni po wystąpieniu objawów | Rozpoznanie niedawnej infekcji | Pojedyncza próbka surowicy sugeruje jedynie możliwość niedawnej infekcji; do potwierdzenia konieczna jest serokonwersja |
| Badanie przeciwciał IgG | Specyficzne przeciwciała IgG | Rekonwalescencja/poprzednia infekcja | Badanie epidemiologiczne, ocena stanu odporności | Pojedyncza próbka surowicy nie nadaje się do diagnozy ostrej dengi |
| Testowanie łączone (NS1+IgM/IgG) | Antygen + Przeciwciała | Pełny przebieg choroby | Kompleksowa diagnostyka zakażenia wirusem denga | Obecnie najskuteczniejszy format RDT do diagnostyki dengi |
| NGS | Wirusowe RNA | 1-7 dni po wystąpieniu objawów | Nadzór genomiczny wirusów | Wymaga specjalistycznego sprzętu do sekwencjonowania i możliwości analizy bioinformatycznej |
4 zalecenia dotyczące testów makro i mikro do wykrywania dengi według scenariusza
W celu wsparcia profilaktyki i kontroli dengi firma Macro & Micro-Test oferuje zintegrowane portfolio diagnostyczne obejmujące szybkie badania przesiewowe, potwierdzenie molekularne i nadzór genomiczny, spełniając potrzeby na różnych etapach zarządzania epidemią.
4.1 Scenariusz 1: Szybkie przesiewanie i ukierunkowany nadzór
Dotyczy klinik gorączkowych, placówek podstawowej opieki zdrowotnej, badań przesiewowych w społecznościach w celu wykrycia ognisk choroby oraz kwarantanny w portach/na granicy.
- Szybki test na antygen NS1 wirusa dengi: wykrywa wczesną infekcję (1–3 dni po wystąpieniu objawów), a wyniki są dostępne już po 15 minutach, co umożliwia szybką selekcję.
- Test na obecność przeciwciał IgM/IgG wirusa dengi: Rozróżnia zakażenia pierwotne i wtórne w celu oceny ryzyka poważnego przebiegu choroby.
- Szybki test łączony na obecność antygenu NS1 wirusa dengi + IgM/IgG: Jednoczesne wykrywanie antygenu i przeciwciał w celu przeprowadzenia pełnej diagnostyki.
- Test na obecność przeciwciał IgM/IgG wirusa Chikungunya: Umożliwia różnicowanie objawów choroby i dokładną identyfikację patogenów.
4.2 Scenariusz 2: Precyzyjna diagnoza i reakcja awaryjna
-Zestaw do wykrywania kwasów nukleinowych wirusa dengi I/II/III/IV: Wykrywa i różnicuje 4 serotypy (limit wykrywalności 500 kopii/ml) w celu śledzenia ognisk choroby.
- Zestaw liofilizowany do PCR w kierunku wirusa dengi: Można go transportować w temperaturze pokojowej, nadaje się do stosowania w obszarach o ograniczonych zasobach i w przypadku nagłych epidemii.
-Zestaw do multipleksowej reakcji łańcuchowej polimerazy w czasie rzeczywistym w kierunku wirusa dengi/ziki/chikungunya: umożliwia jednoczesne wykrywanie 3 arbowirusów, co pozwala na skuteczną diagnostykę różnicową w przypadku złożonych epidemii.

Wszystkie powyższe odczynniki są kompatybilne z całkowicie zautomatyzowanym systemem pobierania próbek i odpowiedzi AIO 800, co pozwala ograniczyć konieczność ręcznej obsługi i ryzyko zanieczyszczenia krzyżowego, a także zwiększyć wydajność i bezpieczeństwo biologiczne.
4.3 Scenariusz 3: Nadzór genomowy i analiza linii wirusowej
Dotyczy krajowych laboratoriów referencyjnych, instytucji badawczych zajmujących się zdrowiem publicznym, zgodnie z pozycjonowaniem NGS przez WHO.
Rozwiązania do nadzoru genomicznego firmy Macro & Micro-Test wspierają sekwencjonowanie całego genomu w celu śledzenia wirusa, wyjaśnienia łańcucha transmisji, monitorowania wariantów i dostosowania strategii szczepień. Wspierają one manualne/automatyczne procesy, zwiększając przepustowość i powtarzalność, umożliwiając laboratoriom przejście od rutynowych testów do zaawansowanego nadzoru, zgodnie z naciskiem WHO na wzmocnienie monitorowania ewolucji wirusów.

4.4 Wartość zintegrowanych rozwiązań
Macro & Micro-Test oferuje kompletne rozwiązania diagnostyczne do wykrywania arbowirusów, wspierając każdy etap zarządzania epidemią: narzędzia do szybkiego przesiewu w placówkach opieki zdrowotnej na pierwszej linii frontu, molekularne potwierdzenie w celu precyzyjnej diagnostyki oraz możliwości analizy całego genomu w celu nadzoru epidemiologicznego. Dzięki wysokowydajnym testom, elastycznym przepływom pracy i platformom gotowym do automatyzacji, rozwiązania te umożliwiają laboratoriom i systemom zdrowia publicznego wzmocnienie gotowości i reagowania na pojawiające się zagrożenia arbowirusowe na całym świecie.
Odniesienia
[1] Światowa Organizacja Zdrowia. Badania laboratoryjne wirusa dengi: wytyczne tymczasowe, kwiecień 2025 r. Genewa: Światowa Organizacja Zdrowia; 2025.
[2] Grupa Doradcza ds. Technicznych Globalnej Inicjatywy Arbowirusowej WHO. Wzmocnienie globalnej gotowości i reakcji na zagrożenia chorobami arbowirusowymi: wezwanie do działania. Lancet Infect Dis. 2026;26(1):15-17.
[3] Lancet Microbe. Pokonywanie dylematu diagnostyki dengi. Lancet Microbe. 2025;6(7):101190.
Czas publikacji: 20 marca 2026 r.
