- 1. Globalny ciężar raka szyjki macicy i wyzwania związane z badaniami przesiewowymi
Rak szyjki macicy pozostaje poważnym globalnym wyzwaniem dla zdrowia publicznego, mimo że można mu w dużej mierze zapobiegać dzięki skutecznym badaniom przesiewowym i wczesnej interwencji. Według Światowej Organizacji Zdrowia (WHO), w 2022 roku na całym świecie odnotowano około 662 000 nowych przypadków i 349 000 zgonów, co plasuje go na czwartym miejscu wśród najczęściej występujących nowotworów złośliwych i czwartej najczęstszej przyczynie zgonów z powodu nowotworów złośliwych wśród kobiet. Obciążenie chorobą jest nieproporcjonalnie skoncentrowane w krajach o niskich i średnich dochodach (LMIC), gdzie wskaźniki zapadalności i śmiertelności są znacznie wyższe niż w krajach o wysokich dochodach. Wynika to przede wszystkim z braku wysokiej jakości programów badań przesiewowych oraz skutecznego wykrywania i leczenia zmian przedrakowych, na co wpływają:
-Brak lub słaba infrastruktura przesiewowa:Brak dostępnych i sprawdzonych jakościowo usług przesiewowych.
-Ograniczenia zasobów:Ograniczona infrastruktura laboratoryjna, logistyka łańcucha chłodniczego i niezawodne zasilanie.
-Niedobory siły roboczej:Brak przeszkolonego personelu laboratoryjnego i klinicznego.
-Opóźnienia i utrata możliwości kontynuacji leczenia:Opóźnienie między pobraniem próbki a udostępnieniem wyników, powodujące opóźnienia w leczeniu klinicznym lub utratę pacjentów z dalszej obserwacji[1].
2. Etiologia i podstawy molekularne karcynogenezy szyjki macicy
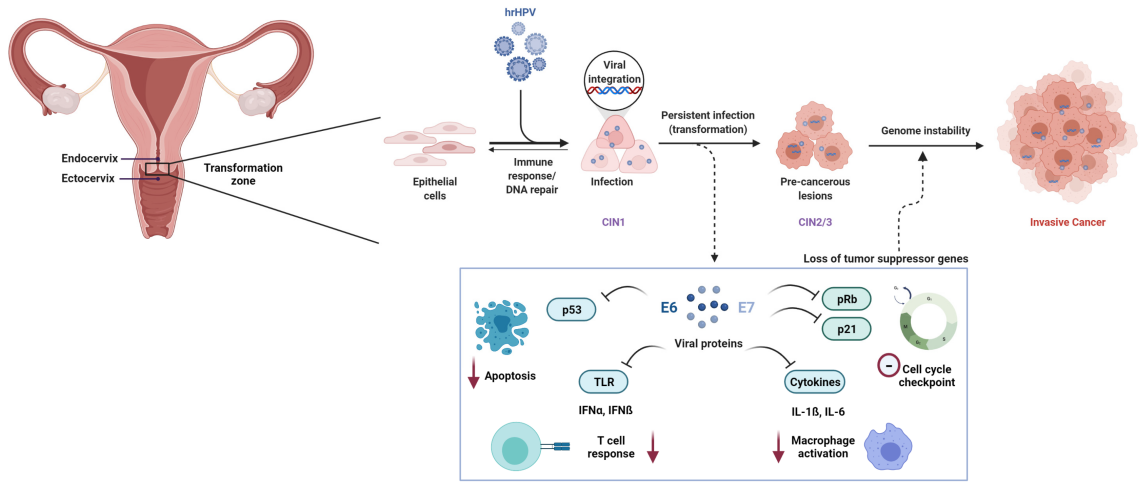
Uporczywe zakażenie wirusem brodawczaka ludzkiego wysokiego ryzyka (HR-HPV) jest nieuchronną przyczyną raka szyjki macicy. Spośród ponad 200 zidentyfikowanych genotypów HPV, co najmniej12 typówzostały sklasyfikowane jako rakotwórcze (Grupa 1) przez Międzynarodową Agencję Badań nad Rakiem (IARC).

Na poziomie molekularnym karcynogeneza indukowana przez HPV jest napędzana głównie przez wirusowe onkoproteiny E6 i E7. E6 promuje degradację białka supresora nowotworu p53, podczas gdy E7 funkcjonalnie inaktywuje białko retinoblastoma (Rb), co prowadzi do zaburzenia regulacji cyklu komórkowego i transformacji nowotworowej.
3.Strategie badań przesiewowych zalecane przez WHO
Światowa Organizacja Zdrowia zaleca badanie kwasu nukleinowego HPV (NAT) jako preferowaną podstawową metodę przesiewową w profilaktyce raka szyjki macicy.
Populacja ogólna:DNA lub mRNA HPV NAT
Kobiety żyjące z wirusem HIV:NAT oparte na DNA HPV
Odstępy między badaniami przesiewowymi:
Kobiety w wieku 30–65 lat: co 5–10 lat
Kobiety żyjące z wirusem HIV: co 3–5 lat
W porównaniu z metodami opartymi na cytologii, testowanie HPV wykazujewyższa wrażliwośći zapewniawyższa negatywna wartość predykcyjna, umożliwiając dłuższe i tańsze odstępy między badaniami przesiewowymi.
4.Profil produktu docelowego WHO dla testów przesiewowych na obecność HPV
WHO opracowałaProfil produktu docelowego (TPP)do badań przesiewowych HPV przeznaczonych do stosowania w środowiskach zdecentralizowanych i o ograniczonych zasobach.[1]
Główne cechy obejmują:
- Zgodność z próbkami pobranymi samodzielnie
- Wykrywanie wielu genotypów HPV wysokiego ryzyka (≥12 typów)
- Obsługa przez personel nieprzeszkolony w laboratorium
- Wyniki dostępne w trakcie jednej wizyty klinicznej
Kryteria te wspierają testy w miejscu opieki oraz strategie „badania przesiewowego i leczenia”.
5.W pełni zautomatyzowana platforma wykrywania wysokiego ryzyka HPV
System AIO800 firmy Macro & Micro-Test zapewniaw pełni zautomatyzowany przepływ pracy od próbki do odpowiedziintegrując ekstrakcję, amplifikację i wykrywanie kwasów nukleinowych zgodnie ze strategiami badań przesiewowych zalecanymi przez WHO.

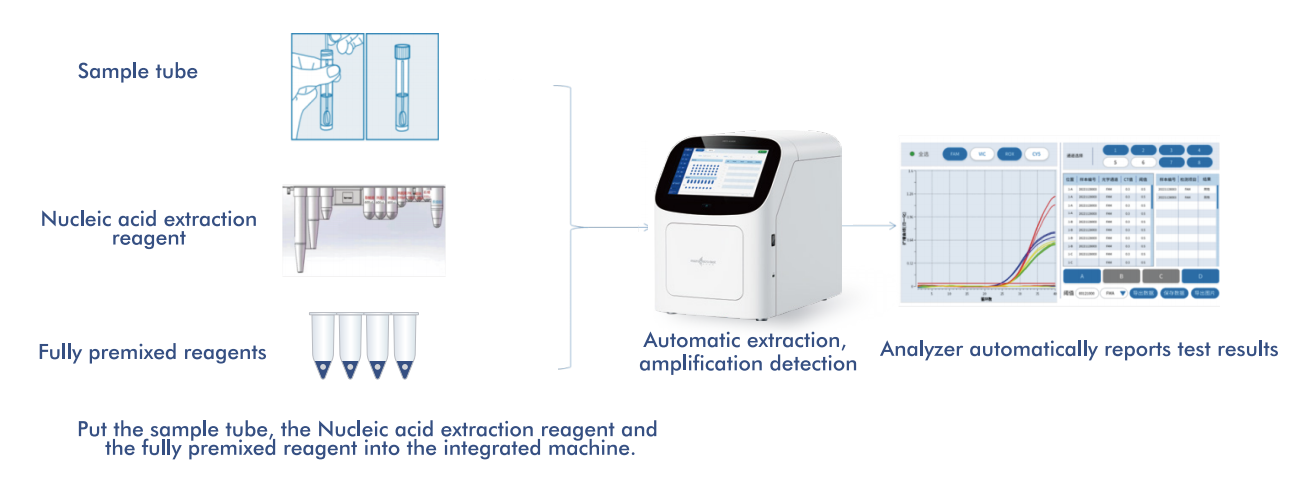
5.1 Zautomatyzowany przepływ pracy od próbki do odpowiedzi
Platforma integruje ekstrakcję, amplifikację i detekcję kwasów nukleinowych w jednym, zamkniętym systemie, wymagającym minimalnej interwencji operatora. Ta konstrukcja:
- -Zmniejsza zależność od wyspecjalizowanego personelu laboratoryjnego
- -Minimalizuje zmienność procesu i ryzyko zanieczyszczenia
- - Umożliwia wdrożenie w zdecentralizowanych placówkach opieki zdrowotnej
Jednocześnie jego przepustowość pozwala na zastosowanie w laboratoriach scentralizowanych, co ułatwia realizację programów badań przesiewowych na szeroką skalę.
5.2 Szeroki zakres genotypowania
System wykrywa 14 typów wirusa HPV wysokiego ryzyka, w tym wszystkie 12 typów rakotwórczych sklasyfikowanych przez IARC (HPV16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 i 59), a także HPV66 i HPV68.
Co ważne, zapewniagenotypowanie specyficzne dla typuwyniki, umożliwiające stratyfikację ryzyka i bardziej precyzyjne zarządzanie kliniczne.
5.3 Czułość analityczna i implikacje kliniczne
Przy limicie wykrywalności 300 kopii/ml system jest w stanie identyfikować zakażenia HPV o niskim poziomie, przyczyniające się do:
- -Wcześniejsze wykrywanie klinicznie istotnych zakażeń
- -Poprawiona wartość predykcyjna ujemna
- - Wsparcie dla wydłużonych odstępów między badaniami
5.4 Obsługa samodzielnego pobierania próbek
Platforma jest kompatybilna z obydwomapróbki wymazów z szyjki macicy i samodzielnie pobrane próbki moczudostosowanie się do zaleceń WHO w celu usunięcia głównych barier utrudniających wykonywanie badań przesiewowych, w tym:
- -Ograniczony dostęp do placówek opieki zdrowotnej
- -Ograniczenia społeczno-kulturowe
Czas publikacji: 27 marca 2026 r.
