Najnowsze badanie opublikowane wMikrobiomprzeprowadził analizę metagenomiki wirusów u 846 dzikich małych ssaków – w tym nietoperzy, gryzoni i ryjówek – zebranych w Sierra Leone w Afryce Zachodniej. W badaniu zidentyfikowano łącznie 39 wirusów RNA związanych z ssakami, w tym 26 nowych i 13 znanych wcześniej wirusów. Spośród nich rodzina Paramyxoviridae charakteryzowała się największą różnorodnością, a gryzonie były nosicielami największej liczby gatunków wirusów (n = 26).
Ocena ryzyka odzwierzęcego ujawniła trzy znane wirusy odzwierzęce – wirus zapalenia mózgu i mięśnia sercowego, wirus Lassa i wirus Rocahepevirus sp. – a także trzy wirusy potencjalnie ryzykujące rozprzestrzenianie się: wirus Melian, wirus zapalenia wątroby gryzoni i wirus Hunnivirus A. Co godne uwagi, spośród nowo zidentyfikowanych wirusów, Bat ledantevirus 2 wykazał najbliższe pokrewieństwo filogenetyczne z wirusem Le Dantec, który zakaża ludzi. Analiza serologiczna dodatkowo wykryła przeciwciała neutralizujące ten wirus u 2,8% mieszkańców, co sugeruje wcześniejsze, prawdopodobnie niewykryte, narażenie ludzi na zakażenie.
Odkrycia te wskazują na obecność znaczącego rezerwuaru wirusów, zdominowanego przez gryzonie, w Afryce Zachodniej i podkreślają kluczowe znaczenie zintegrowanych strategii nadzoru na styku człowiek-zwierzę. Połączenie badań przesiewowych metagenomicznych z walidacją serologiczną zapewnia solidne ramy do identyfikacji wirusów o potencjale zoonotycznym i potencjałem przenoszenia.

W ciągu ostatniej dekady ponad 60% nowo pojawiających się chorób zakaźnych u ludzi pochodziło od zwierząt, a nietoperze, gryzonie i ryjówki uznawane są za głównych nosicieli wirusów odzwierzęcych. Afryka jest powszechnie uważana za ognisko chorób odzwierzęcych. Na przykład, w Sierra Leone odnotowano ponad 28 000 przypadków podczas epidemii eboli w latach 2014–2016.
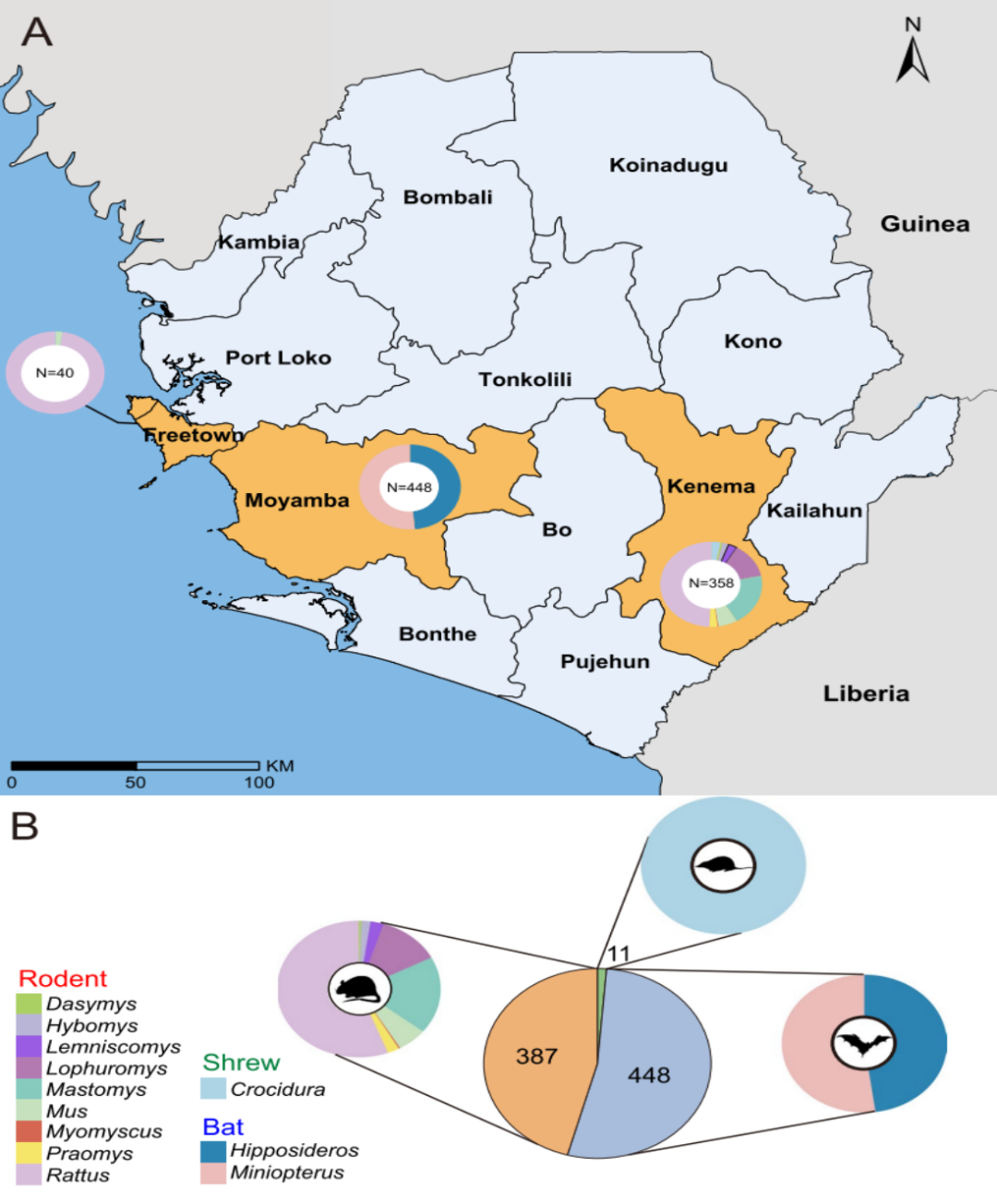
Pomimo znacznego obciążenia chorobami odzwierzęcymi w tym regionie, różnorodność i rozmieszczenie wirusów u dzikich małych ssaków pozostają niedostatecznie poznane. Aby wypełnić tę lukę, naukowcy przeprowadzili systematyczną analizę wiromu 846 dzikich małych ssaków schwytanych w trzech miejscach w Sierra Leone w latach 2018–2023. Celem badania było scharakteryzowanie różnorodności wirusów, identyfikacja kandydatów o potencjale transmisji międzygatunkowej, ocena ryzyka odzwierzęcego oraz wygenerowanie dowodów wspierających systemy wczesnego ostrzegania przed pojawiającymi się chorobami zakaźnymi.
Metody podstawowe
W badaniu zastosowano kompleksowy proces metagenomiki wirusowej:
- Przetwarzanie próbek:Zebrano tkanki serca, wątroby, śledziony, płuc i nerek, połączono je, zhomogenizowano i poddano ekstrakcji całkowitego RNA.
- Sekwencjonowanie i montaż:Przed skonstruowaniem biblioteki przeprowadzono usuwanie rybosomalnego RNA, a następnie sekwencjonowanie o wysokiej przepustowości przy użyciu platformy Illumina NovaSeq 6000. Kontigi wirusowe złożono de novo.
- Identyfikacja wirusa:Wirusy zidentyfikowano na podstawie dopasowania genu polimerazy RNA zależnej od RNA (RdRp). Zachowano jedynie wirusy związane z kręgowcami, z wyłączeniem wirusów bakteryjnych, grzybowych i roślinnych.
- Analiza bioinformatyczna:Przeprowadzono rekonstrukcję filogenetyczną, analizę rekombinacji, modelowanie sieci transmisji międzygatunkowej i ocenę ryzyka odzwierzęcego.
- Walidacja serologiczna:Opracowano test neutralizacji pseudowirusa oparty na VSV dla Bat ledantevirus 2. Przeciwciała neutralizujące wykryto w 2,8% surowic ludzkich, co dostarcza dowodów na potencjalne przeniesienie odzwierzęce.
BadanieWyniki
1. Odkrywanie wirusów i różnorodność
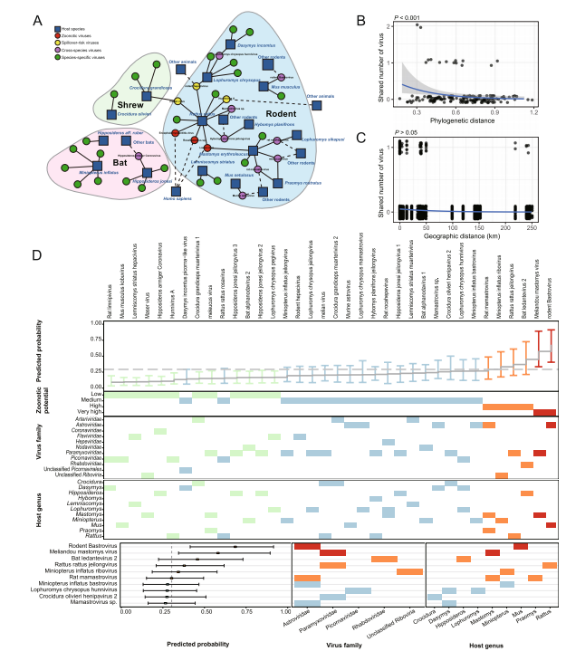
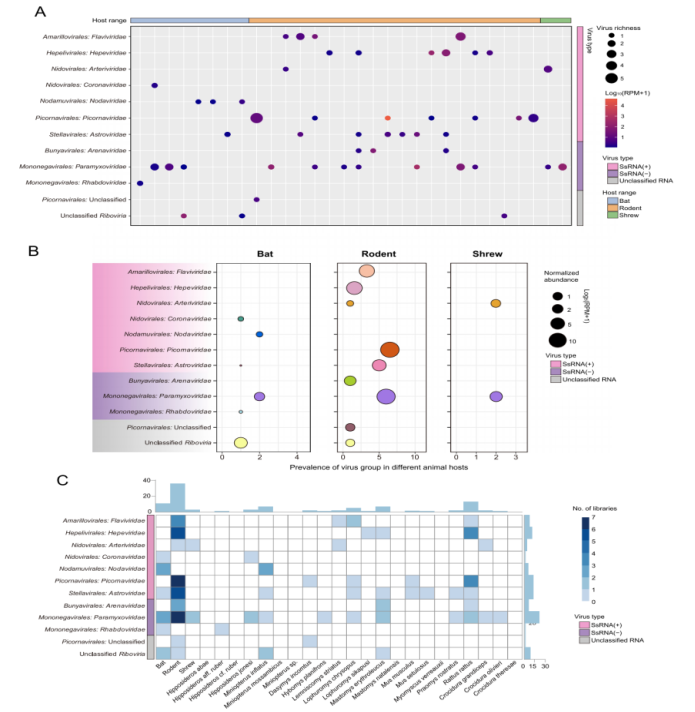
W ramach badania przeprowadzono analizę sekwencjonowania transkryptomowego 846 dzikich zwierząt zebranych w Sierra Leone, w tym gryzoni, nietoperzy i ryjówek. Na podstawie kompletnych sekwencji genu polimerazy RNA zależnej od RNA (RdRp) zidentyfikowano łącznie 39 wirusów RNA związanych z ssakami, w tym 13 wcześniej znanych wirusów i 26 nowych wirusów.
Pod względem składu wirusowego, rodzina Paramyxoviridae charakteryzowała się najwyższym poziomem zróżnicowania we wszystkich trzech rzędach żywicieli, a następnie Astroviridae i Picornaviridae. Jeśli chodzi o dystrybucję żywicieli, gryzonie przyczyniły się do największej różnorodności wirusowej, będąc nosicielami łącznie 26 gatunków wirusów, co wskazuje na ich znaczącą rolę jako rezerwuarów różnorodności wirusowej w regionie.
2. Ryzyko odzwierzęce
Ocena ryzyka odzwierzęcego zidentyfikowała trzy znane wirusy odzwierzęce: wirus zapalenia mózgu i mięśnia sercowego, wirus Lassa i gatunki Rocahepevirus. Ponadto trzy wirusy – wirus Melian, wirus zapalenia wątroby gryzoni i hunnivirus A – zostały zidentyfikowane jako potencjalnie stwarzające ryzyko rozprzestrzeniania się.
Spośród 26 nowo odkrytych wirusów, cztery, na podstawie cech filogenetycznych i genomicznych, przewidywano jako posiadające wysoki potencjał zoonotyczny. Co istotne, Bat ledantevirus 2 wykazał najbliższe pokrewieństwo filogenetyczne ze znanym wirusem Le Dantec, zakażającym ludzi.
Późniejsze badania serologiczne dodatkowo potwierdziły to odkrycie, ponieważ przeciwciała neutralizujące przeciwko Bat ledantevirus 2 wykryto w 2,8% surowic pobranych od lokalnych mieszkańców. Wynik ten sugeruje, że nierozpoznane lub bezobjawowe zakażenia mogły już wystąpić w populacji ludzkiej, co wskazuje na potencjalną, ale wcześniej niewykrytą, odzwierzęcą drogę transmisji.
3. Dynamika transmisji międzygatunkowej
Analiza transmisji międzygatunkowej wykazała, że gryzonie zajmują centralną pozycję w sieci wymiany wirusów, działając jako kluczowe węzły ułatwiające wymianę wirusów między gatunkami żywicieli. Zidentyfikowano łącznie 15 wirusów o potencjale transmisji międzygatunkowej.
Dalsza analiza wzorców transmisji międzyrzędowej wykazała, że dzielenie się wirusami występowało częściej między żywicielami w obrębie tego samego rzędu taksonomicznego, co sugeruje, że pokrewieństwo żywicieli odgrywa istotną rolę w dynamice transmisji. Z kolei nietoperze wykazywały stosunkowo mniejszą zdolność do transmisji międzyrzędowej.
Co istotne, w przypadku niektórych wirusów zaobserwowano dowody na rozszerzenie zasięgu żywicieli. Na przykład wirus Melian, który wcześniej uważano za specyficzny dla ryjówek, został również wykryty w tym badaniu u gryzoni, co wskazuje na potencjalną zmianę w adaptacji żywicieli i zwiększone ryzyko szerszej transmisji.
Wnioski i implikacje dla zdrowia publicznego
- Duża różnorodność wiromów u dzikich małych ssaków:Odkrycie 39 wirusów RNA, w tym 26 nowych gatunków, ujawnia duży rezerwuar wirusów w tym regionie i po raz pierwszy informuje o nowych wirusach o wysokim potencjale odzwierzęcym (np. Bat ledantevirus 2).
- Gryzonie jako priorytetowy cel nadzoru:Gryzonie stanowią główne centra transmisji wirusów i są nosicielami największej różnorodności wirusów, co wiąże się z największym ryzykiem rozprzestrzeniania się wirusa.
- Potrzeba zintegrowanych strategii nadzoru:Wyniki badań potwierdzają, że w programach aktywnego nadzoru należy priorytetowo traktować gryzonie i wdrażać zintegrowane podejścia łączące metagenomikę, serologię i monitoring ekologiczny na styku ludzi i zwierząt.
Ogólnie rzecz biorąc, badanie to dostarcza istotnych dowodów wspierających systemy wczesnego ostrzegania i ramy oceny ryzyka w odniesieniu do nowo pojawiających się chorób odzwierzęcych, podkreślając tym samym znaczenie proaktywnego nadzoru w regionach wysokiego ryzyka.
Informacje o produkcie
Czas publikacji: 23-03-2026