24 marca 2026 roku przypada 31. Światowy Dzień Gruźlicy. Światowa Organizacja Zdrowia (WHO) ogłosiła tegoroczny globalny temat:„Tak! Możemy położyć kres gruźlicy!”, podkreślając, że silne przywództwo rządu, stałe zaangażowanie polityczne i skoordynowane działania międzysektorowe są niezbędne do zakończenia epidemii gruźlicy.

Postęp globalny i pozostałe wyzwania
Według Globalnego Raportu o Gruźlicy 2025 globalna kontrola gruźlicy osiągnęła w 2024 r. znaczący kamień milowy, przy czym zarównozachorowalność i śmiertelność spadająpo raz pierwszy od czasu pandemii COVID-19.
Szacunkowo10,7 miliona ludziW 2024 roku na gruźlicę zachorowało 54% mężczyzn, 35% kobiet i 11% dzieci i młodzieży. Wśród tych przypadków około619 000 (5,8%)byli współzakażeni wirusem HIV i390 000 (3,6%)były gruźlicą wielolekooporną lub oporną na ryfampicynę (MDR/RR-TB).
Gruźlica spowodowała około1,23 miliona zgonówW 2024 r. pozostała główną przyczyną zgonów na świecie, przewyższając COVID-19. Po trzech latach wzrostu zachorowań w latach 2021–2023, globalna zapadalność na gruźlicę spadła o prawie 2% w 2024 r., co odzwierciedla stopniowe odradzanie się usług leczenia gruźlicy.[1]
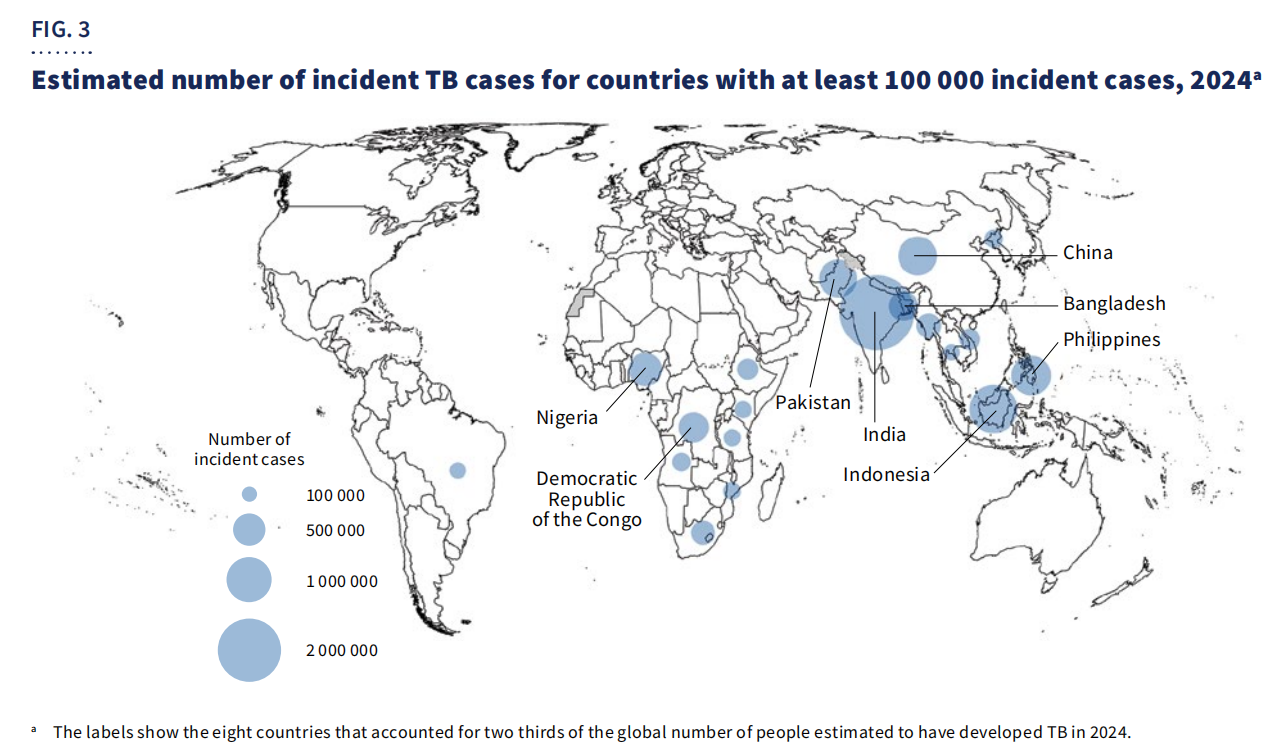
Geograficznie,67% przypadkówbyły skoncentrowane w ośmiu krajach: Indiach, Indonezji, Filipinach, Chinach, Pakistanie, Nigerii, Demokratycznej Republice Konga i Bangladeszu.
Pomimo postępu, gruźlica pozostaje główną przyczyną zgonów wśród osób żyjących z HIV i głównym czynnikiem przyczyniającym się do śmiertelności związanej z opornością na środki przeciwdrobnoustrojowe. Globalne finansowanie wciąż jest niewystarczające, a jedynie5,9 miliarda dolarów amerykańskichdostępne w 2024 r. — znacznie poniżejRoczny cel w wysokości 22 miliardów dolarówzaplanowano na rok 2027.
Dane te podkreślają pilną potrzebę wzmocnienia programów kontroli gruźlicy na całym świecie, ze szczególnym uwzględnieniem zwiększenia dostępu do diagnostyki, poprawy wyników leczenia i zajęcia się czynnikami społecznymi, które napędzają transmisję gruźlicy. Gruźlica nadal wymaga silnej współpracy międzynarodowej i zaangażowania politycznego, aby osiągnąć cele Strategii Eliminacji Gruźlicy.
Mycobacterium tuberculosis: patogeneza i klasyfikacja
Mycobacterium tuberculosis (MTB/M. tuberculosis) jest głównym i najczęstszym patogenem odpowiedzialnym za gruźlicę (TB). Może przedostać się do organizmu człowieka przez drogi oddechowe, przewód pokarmowy lub uszkodzoną skórę i błony śluzowe, infekując wiele narządów i powodując różne postacie gruźlicy. Gruźlica płuc, przenoszona głównie drogą kropelkową, stanowi ponad 80% przypadków gruźlicy. Typowe objawy to kaszel, odkrztuszanie plwociny i krwioplucie. Po zakażeniu płuc bakterie mogą rozprzestrzeniać się drogą krwi do wielu układów, potencjalnie prowadząc do gruźlicy szkieletowej, układu moczowego lub przewodu pokarmowego.[2]
MTB należy do rodzaju Mycobacterium, do którego należą:
- Kompleks Mycobacterium tuberculosis (MTBC): obejmujący m.in. prątki gruźlicy (M. tuberculosis), M. bovis, M. africanum, M. canettii i M. microti. Chociaż prątki gruźlicy są główną przyczyną gruźlicy, to M. bovis i M. africanum mogą również wywoływać tę chorobę.
- Prątki niegruźlicze (NTM).
- Mycobacterium leprae, przyczyna trądu.
Podejścia do diagnostyki laboratoryjnej
Dokładna i terminowa diagnoza jest niezbędna do skutecznej kontroli gruźlicy. Światowa Organizacja Zdrowia podkreśla, żeszybkie technologie diagnostyki molekularnej zasadniczo zmieniły wykrywanie gruźlicy, umożliwiając niezwykle czułą i specyficzną identyfikację patogenów przy jednoczesnym wykrywaniu lekooporności[1].
- Mikroskopia i hodowlae: Hodowla pozostaje złotym standardem w diagnostyce gruźlicy, ponieważ umożliwia ostateczną identyfikację żywych organizmów i wspomaga badania lekowrażliwości oraz analizę genomiczną. Jednak ze względu na powolne tempo wzrostu Mycobacterium tuberculosis, wyniki zazwyczaj pojawiają się po 2–8 tygodniach, co ogranicza jej przydatność kliniczną w podejmowaniu pilnych decyzji.
-Testy immunologiczne: Metody immunologiczne, w tym skórny odczyn tuberkulinowy (TST) i testy uwalniania interferonu gamma (IGRA), wykrywają odpowiedź immunologiczną gospodarza na zakażenie gruźlicą. Chociaż są one przydatne w identyfikacji zakażenia utajonego, testy te nie pozwalają na wiarygodne rozróżnienie zakażenia aktywnego od wcześniejszego, a zatem mają ograniczoną swoistość diagnostyczną w warunkach dużego obciążenia epidemiologicznego.
-Diagnostyka molekularna (NAAT): Zalecane są testy bazujące na DNA, takie jak amplifikacja kwasu nukleinowego (NAAT), ze względu na ich wysoką czułość i swoistość.
-Sekwencjonowanie ukierunkowane nowej generacji (tNGS): Technologie sekwencjonowania ukierunkowanego umożliwiają identyfikację mutacji związanych z opornością o wysokiej rozdzielczości. Wytyczne WHO zalecają tNGS jako zaawansowane narzędzie do wykrywania oporności na leki po diagnozie, wspierające precyzyjne strategie leczenia [3].
-Sekwencjonowanie metagenomiczne nowej generacji (mNGS): Sekwencjonowanie metagenomiczne umożliwia obiektywne wykrywanie szerokiego spektrum patogenów bez konieczności wcześniejszego wyboru celu. To podejście jest szczególnie cenne w złożonych lub niejasnych scenariuszach klinicznych, w tym w przypadku zakażeń mieszanych i pacjentów z obniżoną odpornością, gdzie konwencjonalna diagnostyka może być niewystarczająca.
WHO podkreśla ponadto, że potwierdzenie mikrobiologiczne jest niezbędne do rozpoczęcia odpowiedniej terapii i poprawy wyników leczenia pacjentów, co podkreśla znaczenie integracji zaawansowanej diagnostyki molekularnej z programami kontroli gruźlicy [1].
Kompleksowe rozwiązania diagnostyki molekularnej od Macro & Micro-Test
1.Wykrywanie gruźlicy i lekooporności metodą multipleksowej reakcji PCRgruźlica
| Kod produktu | Nazwa produktu | Orzecznictwo |
| HWTS-RT001 | Zestaw do wykrywania DNA prątków gruźlicy (fluorescencyjna reakcja łańcuchowa polimerazy) | CE |
| HWTS-RT137 | Zestaw do wykrywania mutacji oporności na izoniazyd Mycobacterium Tuberculosis (krzywa topnienia) | CE |
| HWTS-RT074 | Zestaw do wykrywania oporności na kwas nukleinowy i ryfampicynę Mycobacterium Tuberculosis (krzywa topnienia) | CE |
| HWTS-RT102 | Zestaw do wykrywania kwasów nukleinowych oparty na izotermicznej amplifikacji sondy enzymatycznej (EPIA) dla Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Zestaw do wykrywania kwasu nukleinowego kompleksu Mycobacterium Tuberculosis w postaci liofilizowanej (amplifikacja izotermiczna sondy enzymatycznej) | CE |
| HWTS-RT105 | Zestaw do wykrywania liofilizowanego DNA prątków gruźlicy (PCR fluorescencyjny) | CE |
| HWTS-RT147 | Zestaw do wykrywania oporności na kwas nukleinowy Mycobacterium Tuberculosis i ryfampicynę oraz izoniazyd (krzywa topnienia) | CE |
W przypadku silnego klinicznego podejrzenia gruźlicy (TB),HWTS-RT147Test jest zalecany do jakościowego wykrywania zakażenia prątkiem gruźlicy (MTB) i gruźlicy wielolekoopornej (MDR-TB). Test ten identyfikuje mutacje w geniegen rpoB, które prowadzą do oporności na ryfampicynę (RIF) i mutacji wGeny katG i InhA, które są związane z opornością na izoniazyd (INH). Zapewnia wydajny, jednorazowy test na obecność gruźlicy MTB i MDR-TB, z wbudowaną wewnętrzną kontrolą jakości, która minimalizuje liczbę wyników fałszywie ujemnych, gwarantując szybkie i dokładne wyniki.
2.Sekwencjonowanie ukierunkowane PTNseq dla patogenów układu oddechowego i profilowanie oporności
| Kod produktu | Nazwa produktu | Spec. |
| HWKF-TS0001 | Zestaw do wzbogacania genów patogenów zakażeń krwi PTNseq | 24 testy/zestaw |
| HWKF-TS0002 | Zestaw do wzbogacania genów patogennych mikroorganizmów w celu wykrycia infekcji ośrodkowego układu nerwowego PTNseq | 24 testy/zestaw |
| HWKF-TS0003 | Zestaw do wzbogacania genów patogenów infekcji układu oddechowego PTNseq | 24 testy/zestaw |
| HWKF-AT0003 | Zestaw do automatycznej budowy biblioteki wzbogacania (ONT) dla patogennych mikroorganizmów infekcji dróg oddechowych PTNseq | 24 testy/zestaw |
| HWKF-TS0004 | Zestaw wzbogacania genów patogenów zakaźnych o szerokim spektrum działania PTNseq | 24 testy/zestaw |
| HWKF-TS0005 | Zestaw wzbogacania genów patogennych mikroorganizmów zakaźnych PTNseq o ultraszerokim spektrum | 24 testy/zestaw |
| HWKF-TS0151 | Zestaw do typowania Mycobacterium i wzbogacania genu oporności na leki (metoda wielokrotnej amplifikacji) | 24 testy/zestaw |
W przypadku mieszanych zakażeń układu oddechowego (w tym zakażeń górnych i dolnych dróg oddechowych, gruźlicy i przewlekłych chorób układu oddechowego) lub gdy wymagana jest analiza genu oporności na leki (np. w przypadku podejrzenia gruźlicy lekoopornej),Seria PTNseq ukierunkowanej detekcji genów o wysokiej przepustowościmoże być stosowany. Opierając się na zaawansowanej technologii sekwencjonowania ukierunkowanego, PTNseq wykorzystuje ultra-multipleksową reakcję PCR do wzbogacania specyficznych sekwencji docelowych, w połączeniu z sekwencjonowaniem wysokoprzepustowym i technologią nanoporów trzeciej generacji, co umożliwia kompleksową identyfikację patogenów i profilowanie oporności na leki.
System wykorzystuje opatentowane, wysoce swoiste startery do ultra-multipleksowej amplifikacji genów docelowych. Wspierany przez opatentowaną bazę danych i inteligentne algorytmy bioinformatyczne, zapewnia precyzyjną identyfikację patogenów, a także analizę genów oporności na leki i wirulencji. Ukierunkowane wzbogacanie zmniejsza interferencję z DNA gospodarza, poprawiając czułość w próbkach z wysokim udziałem człowieka i umożliwiając skuteczne wykrywanie trudnych celów, takich jak:Mycobacterium tuberculosis, grzyby, bakterie wewnątrzkomórkowe, wirusy RNA oraz geny oporności lub wirulencji.
PTNseq osiąga granicę wykrywalnościjuż od 100 kopii/mli okładki175 powszechnych patogenów układu oddechowego, w tym 76 bakterii, 73 wirusy, 19 grzybów, 7 mykoplazm, a takżeChlamydia, Riketsjai 54 geny oporności na lekiW skład panelu wchodzą:Mycobacterium tuberculosiszłożone i główne prątki gruźlicy.
Seria PTNseq łączy wysoką czułość z opłacalnością, zwiększając wskaźniki wykrywania patogenów i wspierając zindywidualizowaną terapię przeciwdrobnoustrojową, a jednocześnie pomagając w ograniczaniu oporności na środki przeciwdrobnoustrojowe. Zintegrowana z w pełni zautomatyzowanym systemem przygotowania biblioteki sekwencjonowania genów (AIOS), zapewnia usprawnione rozwiązanie szpitalne z czasem realizacji od pobrania próbki do uzyskania wyniku wynoszącym zaledwie 6,5 godziny.

3. Sekwencjonowanie metagenomiczne w celu wykrywania patogenów o szerokim spektrum działania
| Kod produktu | Nazwa produktu | Spec. |
| HWKF-MN0011 | Zestaw do wykrywania patogenów metagenomowych (DNA-Illumina) | 24 testy/zestaw |
| HWKF-MN0018 | Zestaw do wykrywania patogenów metagenomowych (DNA-MGI) | 24 testy/zestaw |
| HWKF-MN0021 | Zestaw do wykrywania patogenów metagenomowych (DNA-ONT) | 24 testy/zestaw |
| HWKF-MN0012 | Zestaw do wykrywania patogenów metagenomowych (RNA-Illumina) | 24 testy/zestaw |
| HWKF-MN0019 | Zestaw do wykrywania patogenów metagenomowych (RNA-MGI) | 24 testy/zestaw |
| HWKF-MN0022 | Zestaw do wykrywania patogenów metagenomicznych (RNA-ONT) | 24 testy/zestaw |
| HWKF-MN0013 | Zestaw do wykrywania patogenów metagenomowych (DNA+RNA-Illumina) | 24 testy/zestaw |
| HWKF-AYM0013 | Zestaw do automatycznej budowy biblioteki do wykrywania patogenów metagenomowych (DNA+RNA-Illumina) | 24 testy/zestaw |
| HWKF-MN0020 | Zestaw do wykrywania patogenów metagenomowych (DNA+RNA-MGI) | 24 testy/zestaw |
| HWKF-MN0023 | Zestaw do wykrywania patogenów metagenomowych (DNA+RNA-ONT) | 24 testy/zestaw |
Gdy diagnoza kliniczna jest niejasna,Wykrywanie genów patogenów mNGS z dużą przepustowościąMożna je wykonać na różnych próbkach pobranych od pacjenta, w tym na płynie z płukania oskrzelowo-pęcherzykowego, plwocinie, wymazach z gardła, krwi, płynie opłucnowym, ropie i próbkach tkanek. To podejście wykorzystuje technologię sekwencjonowania metagenomicznego, w której różne próbki poddawane są ukierunkowanej obróbce wstępnej, a następnie ekstrakcji kwasów nukleinowych za pomocą szklanych kulek i enzymów trawiących ściany komórkowe, co zwiększa wydajność ekstrakcji. Sekwencjonowanie jest dostosowane do wielu platform, zapewniając dużą objętość danych, co przekłada się na lepszą czułość i integralność montażu mNGS. Dane są analizowane za pomocą samodzielnie utworzonej bazy danych i inteligentnych algorytmów wykrywających.ponad 20 000 patogenów, w tym bakterie, grzyby, wirusy i pasożyty, dostarczając informacji o podejrzewanych mikroorganizmach chorobotwórczych. Ta metoda jest odpowiednia dla pacjentów trudnych do zdiagnozowania, w stanie krytycznym lub z obniżoną odpornością, w tym do identyfikacjiMTBzłożonyINTM, a także zakażenia mieszane. Znacząco poprawia wskaźniki wykrywania patogenów i pomaga w ukierunkowanym stosowaniu antybiotyków, umożliwiając precyzyjną diagnostykę infekcji.
Wniosek
Mimo że poczyniono znaczne postępy, gruźlica nadal stanowi poważne wyzwanie dla zdrowia na świecie, zwłaszcza w kontekście lekooporności, luk w finansowaniu i nierównego dostępu do diagnostyki.
WHO podkreśla, że zwiększenie dostępu do szybkiej diagnostyki molekularnej i zaawansowanych technologii sekwencjonowania jest niezbędne do osiągnięcia celów Strategii Zwalczania Gruźlicy. Dzięki ciągłym innowacjom, inwestycjom i globalnej współpracy, wyeliminowanie gruźlicy nie jest już jedynie aspiracją, lecz osiągalnym celem.
Odniesienia:
- Światowa Organizacja Zdrowia. Globalny Raport o Gruźlicy 2024/2025: Diagnostyka i Leczenie.
- Światowa Organizacja Zdrowia. Podręcznik WHO dotyczący wyboru molekularnych szybkich testów diagnostycznych rekomendowanych przez WHO do wykrywania gruźlicy i gruźlicy lekoopornej.
- Światowa Organizacja Zdrowia. Skonsolidowane wytyczne WHO dotyczące gruźlicy: Moduł 3 – Diagnostyka (aktualizacja z 2024 r.).
Czas publikacji: 24-03-2026
