Niedawno czasopismo British Journal of Clinical Pharmacology opublikowało pierwsze wytyczne kliniczne opracowane przez brytyjskie Centrum Doskonałości ds. Nauki Regulacyjnej i Innowacji w Farmakogenomice (CERSI PGx) zatytułowane „Badanie genotypu CYP2C19 dla klopidogrelu: Wytyczne opracowane przez brytyjskie Centrum Doskonałości ds. Nauki Regulacyjnej i Innowacji w Farmakogenomice (CERSI PGx)”. Ten przełomowy dokument koncentruje się na klinicznej wartości genotypowania CYP2C19 w ukierunkowywaniu terapii klopidogrelem.

O CERSI PGx
CERSI PGx to jedno z siedmiu wspieranych przez rząd Wielkiej Brytanii centrów naukowo-innowacyjnych, działających w zakresie regulacji, uruchomionych w styczniu 2025 roku. Centrum, kierowane przez Uniwersytet w Liverpoolu, jest współfinansowane przez Innovate UK, Radę ds. Badań Medycznych (MRC), Agencję Regulacyjną ds. Leków i Produktów Opieki Zdrowotnej (MHRA) oraz Biuro Nauk o Życiu (OLS). Celem centrum jest przyspieszenie bezpiecznej i skutecznej integracji farmakogenomiki (PGx) z Narodową Służbą Zdrowia (NHS) poprzez usunięcie kluczowych barier wdrożeniowych. Niniejsze wytyczne stanowią pierwsze wytyczne kliniczne wydane od czasu utworzenia CERSI PGx.
Dlaczego CYP2C19 ma znaczenie dla klopidogrelu
CYP2C19 jest kluczowym członkiem rodziny enzymów cytochromu P450, odpowiedzialnym za aktywację lub inaktywację metaboliczną wielu leków. Polimorfizmy genetyczne w CYP2C19 prowadzą do istotnych różnic międzyosobniczych w metabolizmie leków, wpływając na ich skuteczność i bezpieczeństwo.
Klopidogrel jest szeroko stosowanym lekiem przeciwpłytkowym w zapobieganiu zdarzeniom zakrzepowym w chorobie wieńcowej, udarze niedokrwiennym, chorobie tętnic obwodowych i migotaniu przedsionków. Jako prolek, klopidogrel wymaga aktywacji metabolicznej przez CYP2C19. Wytyczne klasyfikują pacjentów do grupy ultraszybkiej, szybkiej, normalnej, średnio- i wolno metabolizującej na podstawie genotypu CYP2C19. Nosiciele alleli utraty funkcji (np. CYP2C192 i *3*) – średnio- i wolno metabolizujący – nie mogą skutecznie aktywować klopidogrelu, co prowadzi do niewystarczającego hamowania płytek krwi i zwiększonego ryzyka nawrotu zakrzepicy.
Częstotliwość występowania allelu CYP2C192 wynosi około 15% u Europejczyków, 30% u mieszkańców Azji Południowej i aż 60% u rdzennych mieszkańców Oceanii.
Kluczowe zalecenie: powszechne badanie CYP2C19 w kierunku klopidogrelu
W wytycznych stwierdzono, że niezależnie od wskazania wszyscy pacjenci, u których rozważa się zastosowanie klopidogrelu, powinni zostać poddaniCYP2C19genotypowanie.Na podstawie uzyskanych wyników należy zoptymalizować leczenie przeciwpłytkowe:
-Słabo metabolizującypowinni unikać klopidogrelu i w pierwszej kolejności stosować alternatywne leki, które nie zależą od metabolizmu CYP2C19, takie jak tikagrelor lub prasugrel.
-Osoby o średnim metabolizmienależy również rozważyć alternatywne środki lub dostosowanie schematów leczenia zamiast po prostu zwiększać dawkę klopidogrelu.
W Wielkiej Brytanii klopidogrel został zatwierdzony do wtórnej profilaktyki zdarzeń miażdżycowo-zakrzepowych, w przypadku przemijającego ataku niedokrwiennego (TIA) o umiarkowanym lub wysokim ryzyku lub łagodnego udaru niedokrwiennego, a także w zapobieganiu zdarzeniom miażdżycowo-zakrzepowym i zakrzepowo-zatorowym w migotaniu przedsionków.
Poza klopidogrelem: inne leki, w przypadku których genotypowanie CYP2C19 ma kluczowe znaczenie
Wartość genotypowania CYP2C19 wykracza daleko poza klopidogrel. Jako główny enzym metabolizujący leki, CYP2C19 odgrywa również kluczową rolę w metabolizmie worykonazolu, kilku leków przeciwdepresyjnych i inhibitorów pompy protonowej (IPP). Wiele międzynarodowych i krajowych wytycznych zaleca indywidualizację dawkowania tych leków na podstawie genotypu.
1. Leki przeciwdepresyjne (SSRI)
Selektywne inhibitory wychwytu zwrotnego serotoniny (SSRI) – takie jak sertralina, citalopram i escitalopram – są lekami pierwszego rzutu w leczeniu depresji i są metabolizowane głównie przez CYP2C19. Aktywność enzymu CYP2C19 bezpośrednio determinuje stężenie tych leków w osoczu. Osoby słabo metabolizujące mają klirens leku zmniejszony o 30–60%, co predysponuje je do działań niepożądanych, takich jak wydłużenie odstępu QT i sedacja. Osoby metabolizujące z ultraszybkim metabolizmem często mają subterapeutyczne stężenia w osoczu, co prowadzi do opóźnionej odpowiedzi na leczenie i zwiększonego ryzyka przerwania leczenia.
Wytyczne Konsorcjum Wdrażania Farmakogenetyki Klinicznej (CPIC) z 2023 roku stwierdzają, że osoby ze słabym metabolizmem przyjmujące citalopram lub escitalopram mają zwiększone ryzyko wydłużenia odstępu QT i zalecają zmniejszenie dawki o 50%. Wytyczne Holenderskiej Grupy Roboczej ds. Farmakogenetyki (DPWG) z 2021 roku zalecają, aby osoby ze słabym metabolizmem otrzymywały maksymalną dawkę escitalopramu zmniejszoną o 50%, a osoby z ultraszybkim metabolizmem powinny całkowicie unikać escitalopramu. W przypadku sertraliny, DPWG zaleca dawkę dobową nieprzekraczającą 75 mg u osób ze słabym metabolizmem.
Co istotne, niedawno opublikowany Chiński Konsensus Ekspertów ds. Testów Farmakogenomicznych w Psychiatrii (2025) – opracowany przez Grupę Współpracy Medycyny Precyzyjnej Chińskiego Towarzystwa Psychiatrycznego – zawiera wyraźne zalecenia dotyczące genotypowania CYP2C19. W oświadczeniu konsensusu zaznaczono, że zalecenia dotyczące modyfikacji dawkowania zawarte w międzynarodowych wytycznych, takich jak CPIC i DPWG, dla enzymów metabolizujących leki (w tym CYP2C19) mogą być stosowane w populacji chińskiej. Dlatego genotypowanie CYP2C19 przed rozpoczęciem terapii SSRI (np. escitalopramem) umożliwia optymalizację dawki lub zmianę na alternatywne leki, które nie są metabolizowane przez CYP2C19, co pozwala na osiągnięcie precyzji leczenia, poprawę wskaźników odpowiedzi i zmniejszenie liczby działań niepożądanych.
2. Inhibitory pompy protonowej (IPP)
Inhibitory pompy protonowej – w tym omeprazol, lanzoprazol i pantoprazol – są szeroko stosowane w leczeniu zaburzeń związanych z nadkwaśnością, takich jak choroba refluksowa przełyku i choroba wrzodowa żołądka. Ich metabolizm jest również silnie zależny od CYP2C19. Pacjenci z różnymi genotypami CYP2C19 wykazują znaczną zmienność w reakcji na IPP. Nosiciele alleli utraty funkcji (*2, *3) mają znacznie zwiększoną ekspozycję na lek, co może nasilać hamowanie wydzielania kwasu, ale również zwiększać ryzyko działań niepożądanych. Natomiast osoby z prawidłowym metabolizmem mają stosunkowo niższe stężenia w osoczu i mogą doświadczać słabszego hamowania wydzielania kwasu, chociaż zmienność międzyosobnicza pozostaje znacząca.
Wytyczne CPIC z 2020 roku dotyczące inhibitorów pompy protonowej (IPP) zalecają, aby osoby o ultraszybkim metabolizmie przyjmujące omeprazol lub podobne leki metabolizowały lek zbyt szybko, co skutkuje niewystarczającym stężeniem w osoczu i słabym hamowaniem wydzielania kwasu. U tych pacjentów należy zwiększyć dawkę i monitorować odpowiedź terapeutyczną. U osób o słabym metabolizmie klirens leku jest powolny, a jego stężenie w osoczu może być podwyższone; chociaż skuteczność może być lepsza, zwiększa się ryzyko toksyczności leku. Rozsądnym rozwiązaniem jest redukcja dawki i monitorowanie odpowiedzi. Dlatego u pacjentów rozpoczynających terapię inhibitorami pompy protonowej (IPP) lub u tych, u których występuje słaba odpowiedź lub działania niepożądane, zaleca się genotypowanie CYP2C19 w celu ustalenia indywidualnego dawkowania, optymalizacji skuteczności i minimalizacji działań niepożądanych.
3. Worykonazol
Worykonazol to lek przeciwgrzybiczy o szerokim spektrum działania, stosowany w leczeniu poważnych zakażeń grzybiczych, takich jak inwazyjna aspergiloza. Ma wąskie okno terapeutyczne: nadmiernie wysokie stężenia w osoczu zwiększają ryzyko hepatotoksyczności i zaburzeń widzenia, a niskie stężenia prowadzą do niepowodzenia leczenia. Metabolizm worykonazolu odbywa się głównie za pośrednictwem CYP2C19, a polimorfizmy genetyczne mają istotny wpływ na jego stężenie w osoczu.
W 2016 roku CPIC opublikowało specjalne wytyczne dotyczące CYP2C19 i worykonazolu. Stwierdzono w nich, że u osób z ultraszybkim metabolizmem obserwuje się obniżone minimalne stężenia worykonazolu i często nie udaje się osiągnąć docelowych stężeń terapeutycznych. Osoby ze słabym metabolizmem charakteryzują się podwyższonymi minimalnymi stężeniami i znacznie zwiększonym ryzykiem wystąpienia działań niepożądanych. Wytyczne CPIC zawierają szczegółowe zalecenia dotyczące dawkowania w oparciu o genotyp. Na przykład dorośli z ultraszybkim metabolizmem powinni otrzymywać alternatywne leki pierwszego rzutu, które nie zależą od metabolizmu CYP2C19, takie jak izawukonazol, liposomalna amfoterycyna B lub posakonazol. Dlatego genotypowanie CYP2C19 przed terapią worykonazolem umożliwia indywidualne dawkowanie i zmniejsza częstość występowania działań niepożądanych związanych z lekiem.
Znaczenie kliniczne: Zwiększanie niezawodności leków
Nowo opublikowane wytyczne po raz kolejny stawiają genotypowanie CYP2C19 na czele medycyny precyzyjnej. Należy jednak pamiętać, że kliniczne zastosowania genotypowania CYP2C19 wykraczają daleko poza klopidogrel – od worykonazolu (leku przeciwgrzybiczego) i SSRI (leków przeciwdepresyjnych) po inhibitory pompy protonowej stosowane w celu zmniejszenia kwasowości. Genotyp CYP2C19 działa jak „kompas” w terapii lekowej.
Wraz z rosnącą akceptacją medycyny precyzyjnej, coraz więcej autorytatywnych wytycznych uwzględnia genotypowanie CYP2C19 w rutynowym procesie leczenia. Znajomość własnego genotypu CYP2C19 pomaga pacjentom zrozumieć indywidualny profil odpowiedzi na leki i umożliwia wspólne podejmowanie decyzji z lekarzem w celu opracowania bardziej odpowiedniego planu leczenia. Dla lekarzy uwzględnienie obiektywnych wyników badań genetycznych w decyzjach o przepisie leków stanowi skuteczny sposób na poprawę jakości leczenia i zapewnienie bezpieczeństwa pacjenta.
Makro i mikrotesty'sRozwiązanie do genotypowania CYP2C19
Macro & Micro Test oferuje zestaw do genotypowania CYP2C19 oparty na ulepszonym systemie mutacji opornych na amplifikację (ARMS) w połączeniu z sondami Taqman o następujących cechach:
-Kompleksowe pokrycie alleli– wykrywaCYP2C192, *3 i *17bez pomijania kluczowych wariantów.
-Solidna kontrola jakości– zawiera kontrole negatywne/pozytywne, kontrolę wewnętrzną i enzym UDG do czterostopniowej kontroli jakości w celu zapewnienia dokładnych wyników.
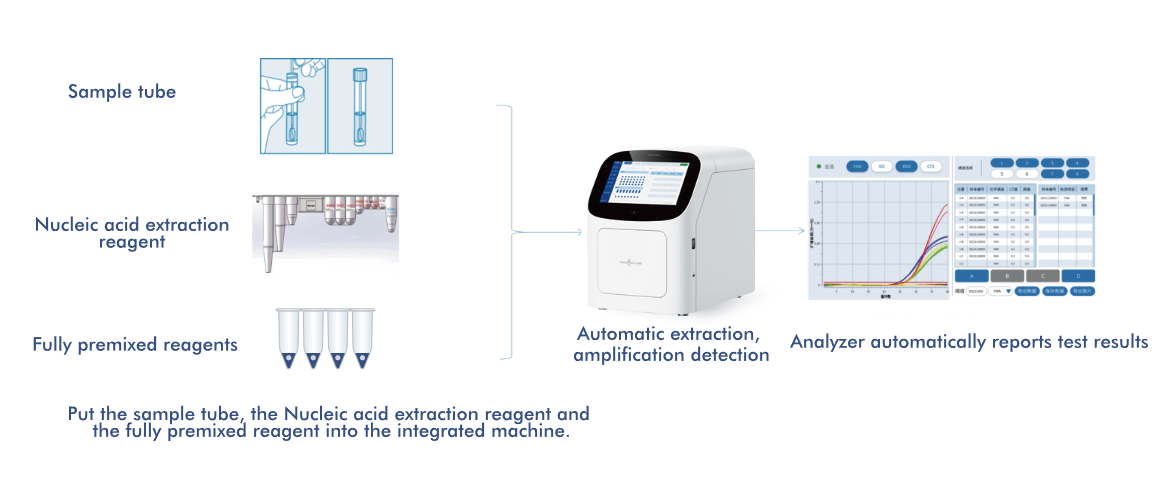
-Automatyczna ekstrakcja– kompatybilny z całkowicie zautomatyzowanym ekstraktorem kwasów nukleinowych firmy Macro & Micro-Test, co zwiększa wydajność przepływu pracy.
-Szeroka kompatybilność– współpracuje z najpopularniejszymi na rynku urządzeniami do PCR w czasie rzeczywistym, w tym ABI 7500 Hongshi SLAN 96P.
-Automatyczna interpretacja wyników– dedykowane oprogramowanie analityczne (na ABI 7500, SLAN 96P itp.) umożliwia automatyczną interpretację wyników, co zwiększa efektywność pracy.
-Automatyzacja gotowa na POCT– W pełni zautomatyzowany analizator amplifikacji kwasów nukleinowych HWTS AIO800 umożliwia działanie na zasadzie „próbka wchodzi, wynik wychodzi”.
Wraz z ciągłym postępem farmakogenomiki, oczekuje się, że genotypowanie CYP2C19 przyniesie korzyści coraz większej liczbie pacjentów, przenosząc medycynę precyzyjną z fazy koncepcyjnej do rutynowej praktyki klinicznej. Niedawno opublikowane wytyczne CERSI PGx podkreślają kluczową rolę badań CYP2C19 nie tylko w przypadku klopidogrelu, ale także rosnącej listy leków, w tym leków przeciwdepresyjnych, inhibitorów pompy protonowej i worykonazolu. Aby ułatwić powszechne stosowanie przepisywania leków na podstawie genotypu, niezbędne są niezawodne i przyjazne dla użytkownika rozwiązania testowe. Oferta testów farmakogenomicznych firmy Macro & Micro-Test, obejmująca kompleksowe pokrycie alleli, solidną kontrolę jakości i platformy gotowe do automatyzacji, ma na celu wsparcie dostawców usług opieki zdrowotnej we wdrażaniu medycyny precyzyjnej i ostatecznie w ochronie zdrowia pacjentów.
Produkty powiązane:
Odniesienia:
1. Lima JJ, Thomas CD, Barbarino J i in. Wytyczne Konsorcjum Wdrażania Farmakogenetyki Klinicznej (CPIC) dotyczące dawkowania inhibitorów CYP2C19 i pompy protonowej. Clin Pharmacol Ther. 2020. doi:10.1002/cpt.20151.
2. Lee CR, Luzum JA, Sangkuhl K i in. Wytyczne Konsorcjum ds. Wdrażania Farmakogenetyki Klinicznej dotyczące genotypu CYP2C19 i terapii klopidogrelem: aktualizacja z 2022 r. Clin Pharmacol Ther. 2022. doi:10.1002/cpt.25261.
3. Narodowy Instytut Zdrowia i Doskonałości Opieki (NICE). Badanie genotypu CYP2C19 w celu ukierunkowania stosowania klopidogrelu po udarze niedokrwiennym lub przemijającym ataku niedokrwiennym. Wskazówki diagnostyczne DG59. Opublikowano: 31 lipca 2024 r.
4. Grupa Współpracy Badawczej w Dziedzinie Medycyny Precyzyjnej Chińskiego Towarzystwa Psychiatrycznego. Konsensus ekspertów dotyczący badań farmakogenomicznych w psychiatrii (2025) [Zhonghua Jing Shen Ke Za Zhi].Chińskie czasopismo psychiatryczne. 2025;58(6):434-445. doi:10.3760/cma.j.cn11366120240611-00181
5. Dello Russo C, Frater I, Kuruvilla R i in. Badanie genotypu CYP2C19 w przypadku klopidogrelu: wytyczne opracowane przez brytyjskie Centrum Doskonałości w zakresie nauk regulacyjnych i innowacji w farmakogenomice (CERSI-PGx). Br J Clin Pharmacol. 2025. DOI: 10.1093/bjcp/…
6. Moriyama B, Owusu Obeng A, Barbarino J i in. Wytyczne Konsorcjum ds. Wdrażania Farmakogenetyki Klinicznej (CPIC) dotyczące terapii CYP2C19 i worykonazolem. Clin Pharmacol Ther. 2017;102(1):45-51. doi:10.1002/cpt.595.
7. Bousman CA, Stevenson JM, Ramsey LB i in. Wytyczne Konsorcjum ds. Wdrażania Farmakogenetyki Klinicznej (CPIC) dotyczące genotypów CYP2D6, CYP2C19, CYP2B6, SLC6A4 i HTR2A oraz leków przeciwdepresyjnych będących inhibitorami wychwytu zwrotnego serotoniny. Clin Pharmacol Ther. 2023;114(1):51-68. doi:10.1002/cpt.2903.
8. Brouwer JMJL, Nijenhuis M, Soree B i in. Wytyczne Holenderskiej Grupy Roboczej Farmakogenetyki (DPWG) dotyczące interakcji gen-lek między CYP2C19 i CYP2D6 a SSRI. Eur J Hum Genet. 2021. doi:10.1038/s41431-021-00894-2.
Czas publikacji: 22-04-2026